Darmstörungen gehen häufig mit subklinischer Neuroinflammation und geistiger Dysbalance einher.
von Keren Grafen
Ein halbes Jahr nach Frau M.s (Name von der Redaktion geändert) Operation waren ihre Beschwerden auf ein schier unerträgliches Maß angestiegen: Fast der komplette Dickdarm war entfernt worden.
Zuvor litt sie chronisch unter starken Bauchschmerzen und Verdauungsproblemen. Eine Untersuchung ergab eine Überlänge des Dickdarms. Nachdem verschiedene Abführmittel keine Erleichterung brachten, empfahlen die behandelnden Ärzte eine operative Dickdarmkürzung.
„Haben Sie schon etwas vom Leaky-Gut- Syndrom gehört?“
Kurze Zeit nach dem Eingriff entwickelte sich eine Dünndarmfehlbesiedelung mit starkem Meteorismus. Die Gabe mehrerer Antibiotika verschlechterte die Symptomatik weiter. Die sich einstellende Niedergeschlagenheit kombiniert mit starken Konzentrations- und Gedächtnisproblemen wurde mit Antidepressiva behandelt.
Vier Darmbarrieren gegen Eindringlinge
Der Darm übernimmt im Körper viele Aufgaben. Neben der Nährstoffaufnahme ist er wesentlich am Immunsystem beteiligt. Um diese Funktionen ausführen, verfügt er über mehrere Barrieren, die sich gegenseitig ergänzen. Dazu zählen insbesondere eine intakte bakterielle Besiedelung (intestinale Mikrobiota), die Bildung von Darmsekreten – hauptsächlich Schleim und sekretorisches IgA – und zahlreiche intramurale (in der Darmwand gelegene) Lymphozyten. Letztere befinden sich überwiegend in den 2–5 cm großen Peyerschen Plaques der Darmwand. Die Epithelschicht bildet zudem durch ihre fest miteinander verbundenen Tight-junction-Proteine eine dicht schließende Barriere.
Passieren trotz dieser Schutzmechanismen Toxine, Bakterien oder Bakterienbestandteile wie Lipopolysaccharide (LPS) den Darm, werden diese zunächst über den Pfortaderkreislauf zu den Kupferzellen der Lebersinusoiden transportiert. Dort können sie über Lebermakrophagen entfernt oder durch chemische Oxidation inaktiviert werden, bevor sie in den Blutkreislauf gelangen. Je besser jedoch die Barrieren des Darmes funktionieren, desto weniger wird die Leber belastet.
Tight junctions: Das Epithel macht dicht
Der (Nähr-)Stofftransport über die Darmschleimhautzellen erfolgt entweder direkt durch die Zellen (transzellulär) oder zwischen ihnen hindurch (parazellulär). Für den parazellulären Transport können sich die Tight junctions (stabile Zellkontakte) der Epithelzellen des Darms wie eine Schleuse öffnen und schließen. Dabei ermöglicht Zonulin (siehe Kasten) als Schleusenwärter einen kontrollierten Durchtritt, denn es erhöht durch Anbindung an spezifische Rezeptoren die Permeabilität des Epithels. Daher dient das Protein auch als Marker (Serum, Stuhl) für das Leaky-Gut-Syndrom. Es gilt: Je höher die Zonulinkonzentration, desto durchlässiger der Darm.
Kurz gefasst
In der Darmschleimhaut und den Gehirnkapillaren verkitten belastbare Proteinverbindungen – Tight junctions – die Epithelzellen zu einer dicht schließenden Barriere gegen unerwünschte Substanzen und Fremdkörper.
Über das Immun- und Stoffwechselsystem stehen die Durchlässigkeit der Darmschleimhaut und der Blut-Hirn-Schranke in enger wechselseitiger Verbindung. Daher gehen Darmstörungen häufig mit subklinischer Neuroinflammation und geistiger Dysbalance einher.
Im Fall Johanna P. konnten massive Darm- und Depressionsbeschwerden mit einer Kombination aus Probiotika, Glutamin, Zink, glutenfreier Ernährung und Bewegung erfolgreich behandelt werden.
Sind die Tight junctions permanent geöffnet, entwickelt sich ein Leaky Gut („durchlässiger Darm“). Dabei kann die intestinale Tight-junction-Fehlfunktion anfänglich nur im Darm lokalisiert sein. Langfristig werden jedoch auch andere Organsysteme beeinträchtigt. In der Regel verschlechtern sich zunächst die Leberwerte, später kann auch die Blut-Hirn-Schranke durch die verstärkte immunologische Antwort durchlässiger werden.
Leaky Gut begünstigt Leaky Brain
Bei einer Störung der Blut-Hirn-Schrankenfunktion spricht man vereinfachend von einem Leaky Brain. Allerdings wird dabei nicht das Gehirn selbst, sondern die Blut-Hirn-Schranke durchlässiger. Unumstritten ist mittlerweile, dass ihre Permeabilität durch einen Leaky Gut ansteigt, sodass verstärkt unerwünschte Stoffe ins Gehirn eindringen. Dies begünstigt oder verursacht möglicherweise sogar die Entstehung zahlreicher neurodegenerativer Erkrankungen wie Demenz oder Morbus Parkinson.
Wechselseitige Einflüsse: Darm-Hirn-Achse
Die komplexen Interaktionen zwischen zentralem Nervensystem und den sympathischen, parasympathischen und enterischen Nervensystemanteilen des Verdauungstrakts werden auch als Darm-Hirn-Achse oder Gut-Brain-Axis bezeichnet. Im Darm sind allein rund 100 Millionen Neuronen lokalisiert, man spricht vom Bauchgehirn oder vom enterischen Nervensystem. Die Darm-Hirn-Achse stellt einen sich rasch entwickelnden Forschungszweig der Neurogastroenterologie dar.
Refresher
Was ist Zonulin?
Zonulin ist ein von Enterozyten sezerniertes Protein und für die Öffnung der Tight junctions verantwortlich. Der Darm kann für einen kontrollierten Durchfluss die Steuerung dieses Proteins nach Bedarf selbstständig regulieren. Zonulin erhöht sich jedoch durch Belastungsfaktoren wie das in Getreide und seinen Produkten enthaltene Gliadin (Teil des Glutens).
Mikroglia-Aktivierung aus dem Darm
M1-Mikrogliazellen werden durch zahlreiche Faktoren wie Zytokine / (im Rahmen von Infektionen oder Autoimmunerkrankungen) angeS lockt und aktiviert. Meist geschieht dies durch proinflammatorische Zytokine wie IFNY (Interferon gamma), TNFα (Tumor-Nekrose-Faktor alpha), GM-CSF (Granulozyte Macrophage Colony Stimulating Factor) und LPS (Lipopolysaccharide). Letztere sind als Toxine in der Zellwand von gramnegativen Bakterien verankert und werden zum Beispiel durch einen Leaky Gut in die Blutbahn ausgeschüttet. LPS gehören zu den pathogenassoziierten molekularen Mustern (PAMP), binden an den Toll-like-Rezeptor 4 (TLR4) und bilden damit die Schnittstelle zwischen angeborenem und erworbenem Immunsystem.
Werden Mikroglia über LPS aktiviert, schütten sie Entzündungsmediatoren wie IL6, TNFα und Proteasen aus. i Außerdem induzieren aktivierte Mikroglia die Sekretion der i induzierbaren NO-Synthase (iNOS), wodurch Stickstoffmonoxid (NO) gebildet wird.
Ganzheitliche Therapeuten kennen schon seit langem einen Zusammenhang zwischen psychischem Stress und gastrointestinalen Störungen wie Reizdarmsyndrom, Morbus Crohn oder Colitis ulcerosa. Dieser ist mittlerweile aus zahlreichen Studien belegt: Stress verändert unmittelbar die intestinale Permeabilität sowie die Immunfunktionen des Darmes. Aber auch umgekehrt beeinflusst der Verdauungstrakt Emotionen, Schmerzempfindung und die Funktion der Blut-Hirn-Schranke.
Wächter der Hauptzentrale: Blut-Hirn-Schranke
Das Gehirn ist durch die Blut-Hirn-Schranke einer der bestgeschützten Bereiche des Körpers. Die Endothelzellen der Kapillarwand mit ihrer Basalmembran dienen hierbei als wichtigste Barriere. Im Gegensatz zu den Endothelzellen der Peripherie sind sie mit 0,3–0,5μm sehr klein, besitzen keine Fenestrierungen (Poren), aber die fünf- bis zehnfache Zahl an Mitochondrien. Ihre Tight junctions schließen im Gehirn noch deutlich dichter als im Darm. Zusätzlich umhüllen Astrozyten und Perizyten die Kapillaren. Durch diese Barrierefunktion können nur ausgewählte Stoffe aus dem Blutkreislauf ins Gehirn gelangen.
Krankheitserreger, Toxine- sowie Botenstoffe und sogar Immunzellen können die Blut-Hirn-Schranke nicht überwinden. Entzündungen können jedoch alle vier Barriereschichten – Basalmembran, Endothelzellen, Astrozyten und Perizyten – beeinträchtigen: Die Tight junctions werden poröser. Die Astrozyten lassen einen höheren Wassereinstrom zu und blähen sich auf. Die Perizyten verlieren hingegen an Größe, während sich die Basalmembran verdickt. So können Entzündungsmediatoren oder Bakterientoxine (zum Beispiel Pneumokokken) die Tight- junctions-assoziierten Proteine Claudin und Occludin so verändern, dass eine Passage von Zellen (zum Beispiel Erreger, Granulozyten) oder unerwünschten Stoffen ins Gehirn möglich wird.
Abwehr ohne Entzündung: Das besondere Immunsystem des Gehirns
Die hermetische Abschirmung des Gehirns über die Blut-HirnSchranke hat einen besonderen Grund: Das zerebrale Immunsystem ist verhältnismäßig schwach und funktioniert ganz anders als das des übrigen Körpers: Dort zerstört ein Heer von Immunzellen eingedrungene Krankheitserreger und zum Teil umliegendes Gewebe mit akuten Entzündungsreaktionen. Gehen dabei Körperzellen zugrunde, können sich diese in der Regel nach kurzer Zeit neu bilden. Nicht so im Gehirn: Nervenzellen speichern Informationen und sind nicht regenerationsfähig. Ein Zelluntergang würde auch die mit ihrer Hilfe gespeicherten Informationen löschen und wäre nicht reversibel.
Daher läuft jede Immunreaktion im Gehirn streng kontrolliert ab. Durchbrechen unerwünschte Fremdkörper die Blut-Hirn-Schranke, werden Mikrogliazellen als Träger der zerebralen Immunabwehr aktiv. Zu Beginn eines solchen Prozesses wandern aktivierte Ml-Mikrogliazellen zu den eingedrungenen Antigenen, um diese zu eliminieren und den beschädigten Bereich zu reinigen. Sie dosieren ihre Zellgifte wie Sauerstoffradikale, Zytokine und Enzyme (Proteasen) äußerst diskret, um keine Nervenzellen zu verletzen. Ist diese Aufgabe erfüllt, kommt es zu einem immunologischen Shift: Während Ml-Mikrogliazellen ihre Arbeit einstellen, werden entzündungshemmende M2-Mikrogliazellen stimuliert. Wenn also eine geregelte Umschaltung vom Ml - zum M2-Phänotyp stattfindet, kann der Schaden effizient repariert werden.
Bremsen defekt: Neuroinflammation durch Leaky Gut
Bei größeren oder persistierenden Angriffen auf das Gehirn wie durch ein Leaky Gut besteht die Aktivierung der Ml-Mikroglia fort. Die Menge ausgeschütteter Zellgifte und reaktiver Sauerstoffspezies ist nun so hoch, dass auch Nervenzellen angegriffen und zerstört werden. Der M1-/M2-Shift findet nicht mehr statt. Im Rahmen eines Notfallprogramms fordert nun das Gehirn über die Aussendung von Botenstoffen Hilfe aus dem körpereigenen Immunsystem an. Damit dessen Zellen jedoch dorthin gelangen können, wird die Barrierefunktion der Blut-HirnSchranke noch weiter herabgesetzt. Jetzt können sich unter anderem T-Zellen durch die Tight junctions quetschen, um zum Ort des Geschehens kommen. Eine Entzündungsreaktion des zentralen Nervensystems, die Neuroinflammation, beginnt. Diese geschieht zunächst ohne die klassischen Entzündungszeichen wie Rötung, Schwellung, Schmerz oder Überwärmung, da es sich zwar um eine chronische, aber dennoch subklinische Entzündung handelt. Man spricht auch von Silent Neuroinflammation. Was ursprünglich als gesunde Schutzreaktion gegen Krankheitserreger angelegt war, wird jetzt zur Gefahr für das Gehirn. Nervenzellen nehmen irreversibel Schaden. Die klinische Symptomatik ist dabei abhängig vom anatomischen Ort und dem Ausmaß der Zellschädigung durch die Mikroglia. Sie reicht von milden kognitiven Defiziten, Wortfindungsschwierigkeiten, Konzentrationsproblemen, Störungen des Kurzzeitgedächtnisses und der Orientierung bis hin zu gravierenden neurologischen Störungen wie Morbus Alzheimer, Morbus Parkinson, Multiple Sklerose, Zwangsstörungen und Depressionen. Sowohl für die Pathogenese als auch für die Therapie steht die Neuroinflammation im Zentrum der jüngsten Forschung.
Bei zerebralen Beschwerden an den Darm denken
Nicht alle Therapeuten kennen die möglicherweise weitreichenden und zum Teil irreversiblen Folgen eines Leaky-Gut-Syndroms für das Gehirn. Man sollte jedoch bei Symptomen zerebraler Beeinträchtigung wie Konzentrations- und Gedächtnisstörungen, Schwindel, Müdigkeit oder Reizempfindlichkeit immer auch an eine erhöhte intestinale Permeabilität denken. Dies gilt auch bei Morbus Parkinson, Multiple Sklerose, Autismus und kindlicher Hyperaktivität. Häufig sind diese Störungen mit entzündlichen Darmerkrankungen, Durchfall, Obstipation, Meteorismus oder einem Reizdarmsyndrom mit Nahrungsmittelunverträglichkeit oder Zöliakie assoziiert. In der Vorgeschichte gibt es häufig Behandlungen mit Antibiotika oder NSAR (nichtsteroidale Antirheumatika) oder regelmäßigen Alkoholkonsum.
Diagnostik: Zonulin als Leitmarker
Bei der Analyse des Zonulinspiegels kann die Darmpermeabilität ohne den Aufwand einer Provokation (zum Beispiel durch einen Laktose-Mannitol-Test) gut untersucht werden und eignet sich für Verlaufskontrollen zur Wirksamkeit von Therapien und Ernährungsumstellungen. Zur Absicherung der Diagnose können zusätzlich weitere Marker bestimmt werden (siehe Tabelle 1).
Erst Leaky Gut, dann Mikrobiota behandeln
Bei einem Leaky-Gut-Syndrom sollte man zunächst dafür sorgen, dass sich die Tight junctions wieder schließen. Eine Therapie beginnt in meiner Praxis immer mit einer Reduzierung von stark verarbeiteten Lebensmitteln, Zucker und Weißmehlprodukten sowie einer Alkoholkarenz. Auch sollten toxische Arzneimittel und allergieauslösende Nahrungsmittel gemieden oder reduziert werden.
Eine wichtige Rolle beim Schutz der Darmschleimhaut spielt die Aminosäure Glutamin. Sie dient als zentraler Energielieferant des Dünndarmepithels sowie als Hauptsubstrat in der Glutathionsynthese und spielt eine enorme Rolle bei der Abwehr freier Radikale. Glutamin fördert auch die Regeneration der Dünndarmschleimhaut und verhindert den Abbau der Tight junctions, insbesondere in Kombination mit Zink.
Zu den wichtigsten Glutaminlieferanten zählen eiweißreiche Lebensmittel wie Käse (ca. 7 g/100 g), Geflügel oder Fisch, aber auch Gemüse wie Hülsenfrüchte (Linsen: 4,5 g/100 g), Kartoffeln und Rettich. Unter normalen Umständen erhält der Körper durch eine ausgewogene Ernährung ausreichend Glutamin. Bei einem Leaky Gut kann eine höhere Zufuhr sinnvoll sein, um die Syntheseleistung der wichtigsten Tight-junction-Proteine Occludin und Claudin zu erhöhen. Dies ist die in der Regel nur über Nahrungsergänzungsmittel zu erreichen. Wie hoch Glutamin zu dosieren ist, hängt von Alter, Gesundheitszustand und anderen Faktoren wie erhöhter sportlicher Aktivität ab. Für einen Erwachsenen geht man durchschnittlich von einer Tagesdosis von l0 g aus. Auch Frau M. erhielt zu Beginn der Therapie 10 g Glutamin sowie 25 mg Zink pro Tag p.o.
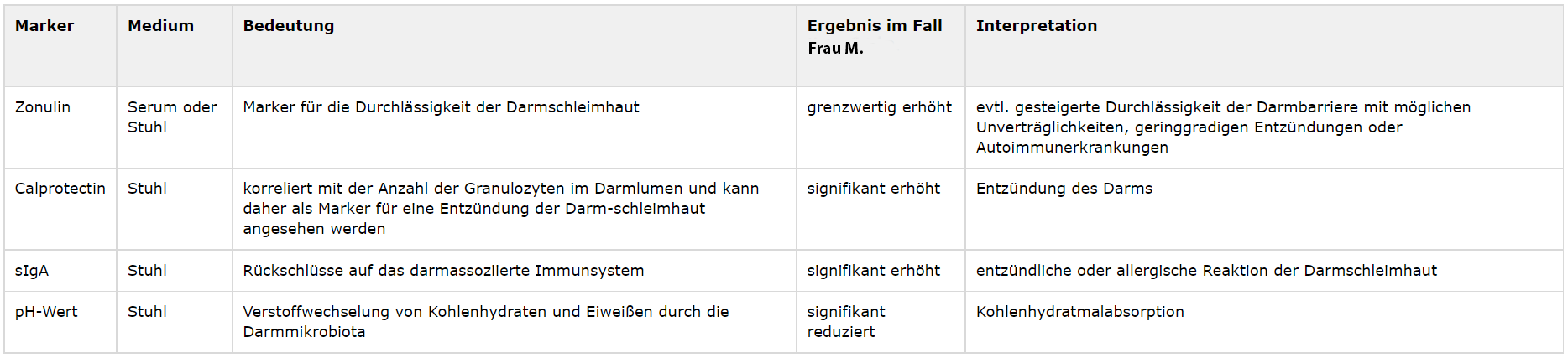
Tab. 1 Wichtige Marker bei Leaky Gut
Für Dauertherapie geeignet: Pro- und Präbiotika
Nach der Ernährungsumstellung ist die Einnahme von Pro- und Präbiotika sinnvoll. Probiotika sind Lebensmittel oder Supplemente mit lebenden Mikroorganismen, in der Regel Bakterien oder Hefen. Präbiotika enthalten hingegen keine lebenden Organismen, sondern regen das Wachstum oder die Aktivität vorhandener Darmbakterien an.
Ob sich das Mikrobiom nach einer mehrwöchigen Therapie tatsächlich nachhaltig regeneriert hat, hängt von mehreren Faktoren ab. Grundsätzlich gilt: Wer seinen Darm dauerhaft gesund halten möchte, sollte Pro- und Präbiotika täglich in den Speiseplan integrieren, und zwar auf Lebenszeit. Die medikamentöse Therapie in Kapselform erfolgt so lange, bis sich die Symptome deutlich verbessert haben, meist über 3–9 Monate.
Frau M. erhielt das Präparat ProBio-Cult® Relax (Fa. Syxyl). Dabei handelt es sich um ein Kombipräparat aus Vitamin Bj, B3, B6 und B12 (Nervenfunktion und Psyche), Pantothensäure (Leistungsfähigkeit) und L-Tryptophan (Serotoninvorstufe), sechs verschiedenen Lactobacillus- und Bifidokulturen sowie resis- tenter Stärke als Präbiotikum.
Auf Dauer lassen sich über die Ernährung in der Regel ausreichend Prä- und Probiotika zuführen, insbesondere über naturbelassenen Joghurt und fermentiertes Gemüse wie Sauerkraut. Zu den natürlichen Präbiotika zählen Nahrungsinhaltsstoffe wie Inulin, das unter anderem in Chicorée, Topinambur, Artischocken, Knoblauch und Zwiebeln enthalten ist.
Psychobiotika: Bakterien für die Seele
Angesichts des zunehmenden Wissens über die Interaktion von Darmmikrobiom, Psyche und Gehirnfunktion werden einige Probiotika heute als Psychobiotika bezeichnet. Es handelt sich dabei um Mikroorganismen wie Lactobacillus und Bifidobakterien, die sich nicht nur auf die Regulierung der Darmtätigkeit, sondern auch auf Psyche und Gehirnfunktion positiv auswirken. Psychobiotika können die Synthese beziehungsweise den Wirkungsgrad von Neurotransmittern wie Serotonin, Dopamin und Gamma-Amino-Buttersäure (GABA) beeinflussen. Mensehen mit Depressionen und anderen psychischen Erkrankungen können somit von einer Behandlung mit psyehobiotisehen Darmbakterien profitieren, wie zahlreiche Studien zeigen. Die Neurogastroenterologie als zuständiges, junges Fachgebiet eröffnet daher zunehmend neue Therapiemöglichkeiten.
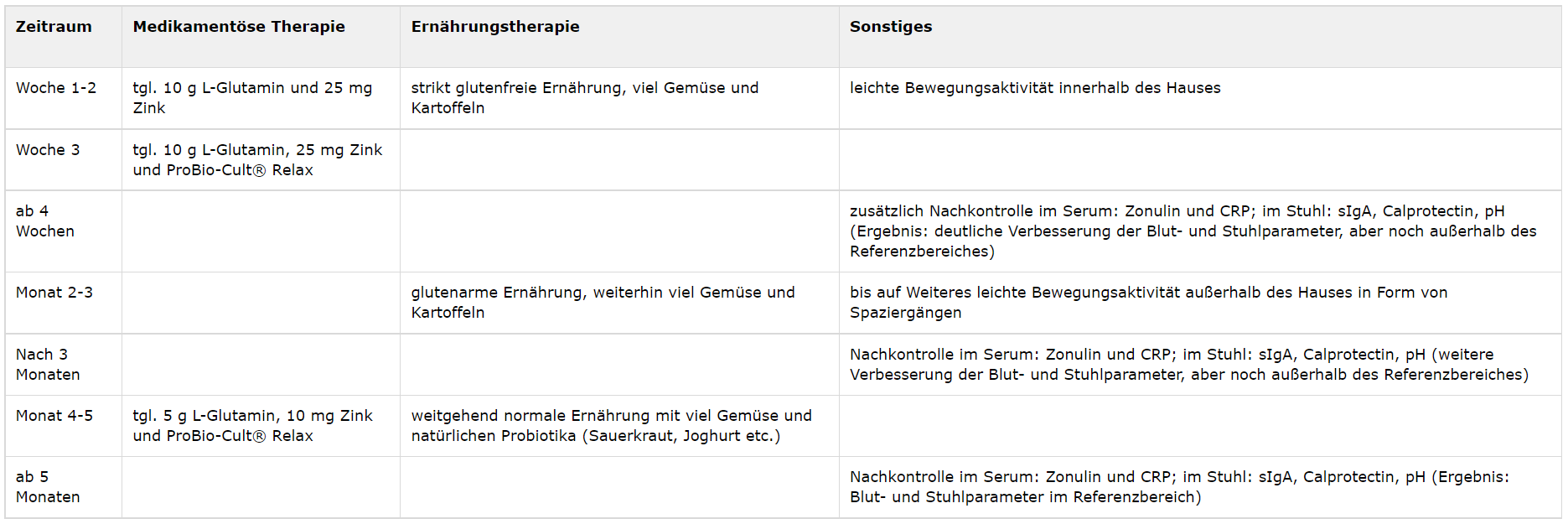
Tab. 2 Therapeutisches Vorgehen bei Frau M.
Fallbericht: Besserung nach Ernährungsumstellung und Probiotika
Nachdem ich bei Frau M. einen Leaky Gut und ein stark fehlgeleitetes Immunsystem diagnostiziert hatte, begannen wir sofort mit einer Therapie, die auf mehreren Komponenten aufbaute. Neben den Medikamenten und der Ernährungstherapie empfahl ich Frau M. auch regelmäßige Bewegungsaktivität, zunächst zu Hause, später, als sich ihr Zustand zunehmend verbesserte, auch außerhalb des Hauses in Form von Spaziergängen.
Schon nach kurzer Zeit besserten sich Frau M.s körperliche Beschwerden. Im Verlauf der nächsten Monate hielt sie sich strikt an die Ernährungsumstellung und baute Prä- und Probiotika in ihren täglichen Speiseplan ein. Sie beschreibt sich heute wieder als glücklich. Ihre körperlichen Beschwerden und kognitiven Defizite besserten sich in den letzten fünf Monaten deutlich, wenngleich sie nicht vollständig verschwanden. Heute geht sie gern nach dem Essen spazieren. Vor einigen Monaten wäre das für sie noch undenkbar gewesen.
Autorin
Dr. rer. nat. Keren Grafen
Neurobiologin und Heilpraktikerin
Interessenkonflikt: Die Autorin gibt an, dass kein Interessenkonflikt besteht.
Literatur
[1] Foster JA, McVey Neufeld KA.. Gut-brain axis: how the microbiome influences anxiety and depression.. Trends Neurosci 2013; 36 (05) 305-12
[2] Naseribafrouei A. et al. Correlation between the human fecal microbiota and depression.. Neurogastroenterol Motil. 2014; 26 (08) 1155-62
[3] Mayer EA, Padua D, Tillisch K.. Altered brain-gut axis in autism: comorbidity or causative mechanisms?. Bioessays 2014; 36 (10) 933-9
[4] Song Y, Liu C, Finegold SM.. Real-time PCR quantitation of clostridia in feces of autistic children.. Appl Environ Microbiol. 2004; 70 (11) 6459-65
[5] Koloski NA. et al. The brain-gut pathway in functional gastrointestinal disorders is bidirectional: a 12-year prospective population-based study.. Gut 2012; 61 (09) 1284-90